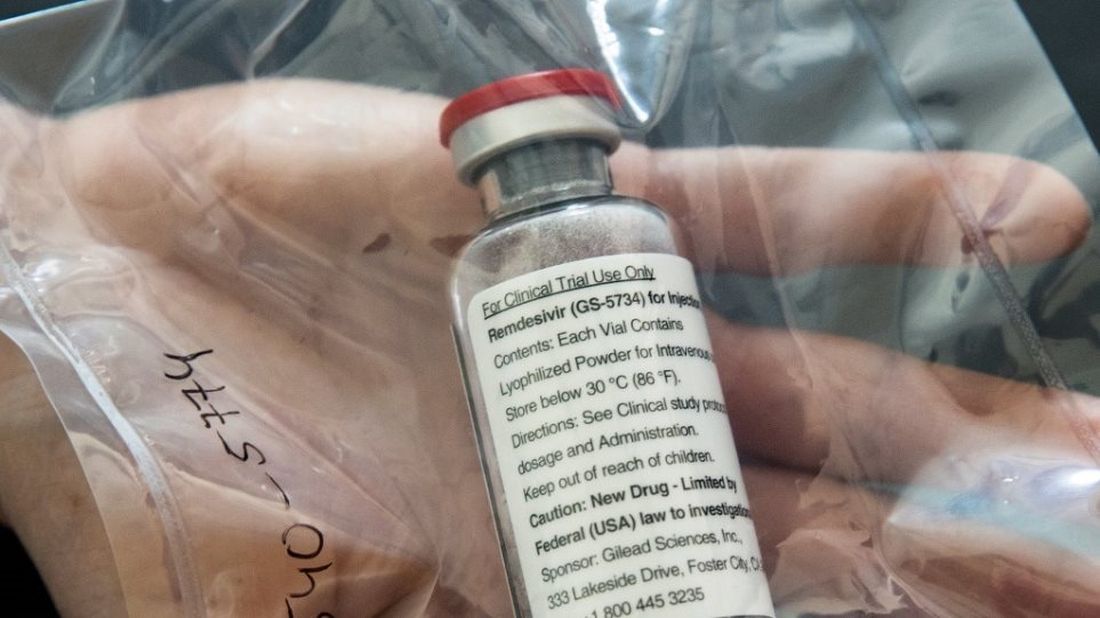
Η Επιτροπή Φαρμακευτικών Προϊόντων για Ανθρώπινη χρήση (CHMP) της Ευρωπαϊκής Επιτροπής συνέστησε σήμερα την υπό όρους έγκριση της ρεμντεσιβίρης, για τη θεραπεία ασθενών με λοίμωξη COVID-19.
Η θετική γνωμοδότηση της CHMP καθιστά το αντι-ιικό φάρμακο της Gilead Sciences το πρώτο φάρμακο για χρήση σε ενήλικες και εφήβους ασθενείς που λαμβάνει το πράσινο φως για έγκριση στην ευρωπαϊκή ήπειρο.
Ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) σε ανακοίνωσή του που εξεδόθη σήμερα αναφέρει ότι η CHMP συστήνει την χρήση της ρεμντεσιβίρης σε ενηλίκους και εφήβους (από 12 ετών και άνω) με πνευμονία που χρήζουν αναπνευστικής υποστήριξης με οξυγόνο.
Η θετική γνωμοδότηση των ευρωπαϊκών αρχών έρχεται λίγες εβδομάδες μετά την fast-track αξιολόγηση του αντι-ιικού φαρμάκου, δίνοντας τη δυνατότητα στους κλινικούς γιατρούς να την συνταγογραφήσουν όπως γίνεται και με άλλα φάρμακα. Εφόσον λοιπόν λάβει την έγκριση κυκλοφορίας από την ΕΕ, θα πωλείται υπό την εμπορική ονομασία Veklury, χωρίς προς το παρόν να έχει γίνει γνωστό κάτι για την τιμή του σκευάσματος.
Αξίζει πάντως να σημειωθεί ότι, η υπό όρους έγκριση σκευασμάτων στην ΕΕ επιτρέπει σε μια θεραπεία να πωλείται για 12 μήνες και στα 27 κράτη-μέλη προτού διατεθούν όλα τα απαραίτητα δεδομένα σχετικά με την αποτελεσματικότητα και τις παρενέργειες του. Η Gilead πρέπει να υποβάλει τα τελικά στοιχεία για το αντι-ιικό έως τον προσεχή Δεκέμβριο.
Η ζήτηση για ρεμντεσιβίρη έχει αυξηθεί λόγω των προκαταρκτικών στοιχείων κλινικών δοκιμών για την αποτελεσματικότητά του στη διαχείριση της COVID-19. Η Gilead αναμένει ότι η διαθεσιμότητα της ρεμντεσιβίρης θα ξεπεράσει τα δύο εκατομμύρια δόσεις μέχρι το τέλος του έτους, διπλασιάζοντας τον προηγούμενο στόχο της και σχεδιάζει να ξεκινήσει κλινική δοκιμή μιας εισπνεόμενης εκδοχής της. Σήμερα χορηγείται μόνο ενδοφλεβίως.
Υπενθυμίζεται ότι το αντι-ιικό έχει ήδη εγκριθεί για επείγουσα χρήση σε ασθενείς με σοβαρή COVID-19 στις Ηνωμένες Πολιτείες Αμερικής, την Ινδία και τη Νότια Κορέα και έχει λάβει πλήρη έγκριση στην Ιαπωνία.